Cardiopatías congénitas
¡ATENCIÓN! Esta página no es un consultorio médico. Los contenidos sobre cuestiones médicas aquí expuestos están documentados a partir de otras fuentes cuya exactitud o veracidad no podemos garantizar. Si quiere resolver alguna duda de carácter médico, le recomendamos que contacte directamente con un profesional de la salud cualificado.
¿Qué son las cardiopatías congénitas?
De forma genérica, una cardiopatía es una patología que afecta al corazón. Las cardiopatías pueden ser adquiridas o congénitas. En el primer caso, la patología surge en un corazón sano en algún momento de la vida, después del nacimiento. Infecciones, como la fiebre reumática o problemas cardiovasculares ligados a diabetes, hipertensión u obesidad, son las principales causas de estas dolencias, mucho más frecuentes en adultos que en niños.
Sin embargo, las cardiopatías congénitas (CC) surgen durante el desarrollo embriológico, por lo que se nace con ellas. Se deben a un error en la formación del corazón o de los vasos sanguíneos circundantes y afectan a 8 de cada 1.000 niños en España.
Las cardiopatías congénitas pueden ser de muchos tipos, pero básicamente están vinculadas a problemas en:
- Las conexiones entre vasos y cavidades del corazón
- El desarrollo completo de todos los vasos y cavidades del corazón
- La formación de las válvulas que impiden el retorno del flujo sanguíneo
- La formación del miocardio ventricular, el músculo que bombea la sangre
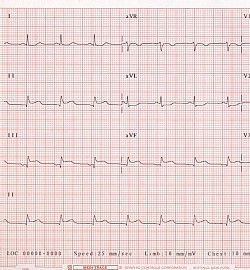
- El funcionamiento del sistema eléctrico del corazón, responsable de activar el miocardio
Afortunadamente, y a diferencia de lo que venía ocurriendo años atrás, cuando muchos bebés que nacían con cardiopatías congénitas morían, actualmente el 85% de las personas llegan a la edad adulta y llevan una vida prácticamente normal, gracias a los avances técnicos de diagnóstico y médico-quirúrgicos.
Tipos de cardiopatías congénitas más frecuentes
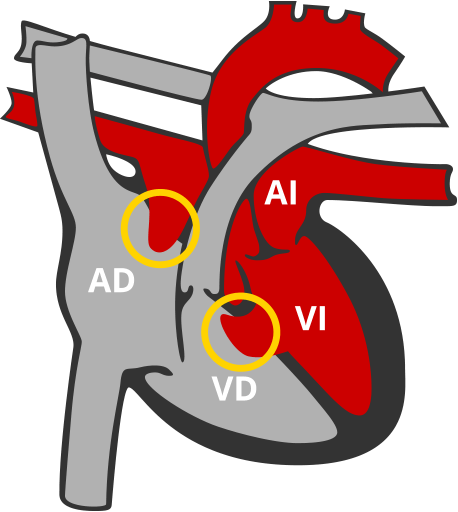
Canal Auriculo-Ventricular (A-V)
Abertura que comunica la totalidad de la parte izquierda y derecha del corazón.
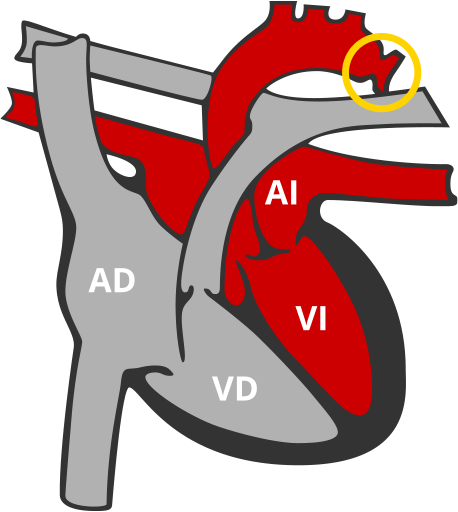
Coartación de Aorta (CoA)
Estrechamiento de la arteria que distribuye la sangre por el cuerpo.
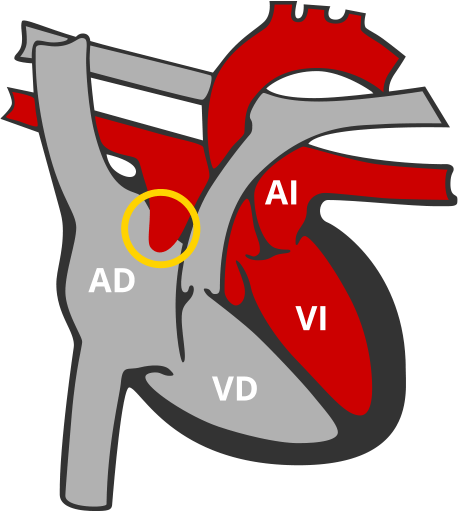
Comunicación Interauricular (CIA)
Abertura que comunica la parte izquierda y derecha del corazón por su parte superior.
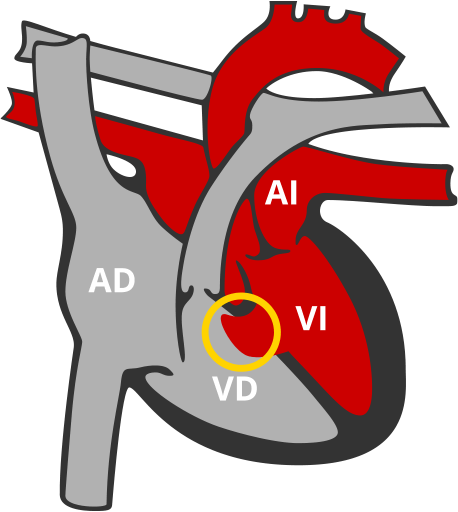
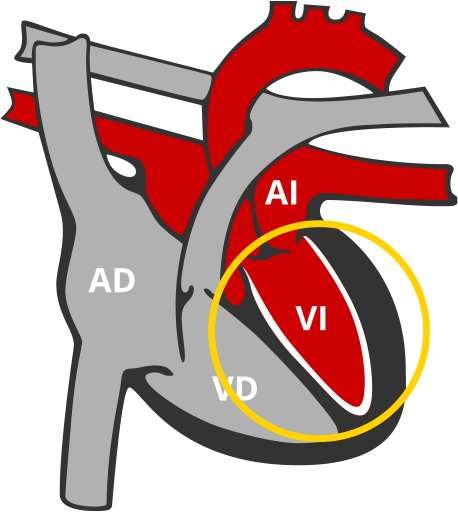
Comunicación Interventricular (CIV)
Abertura que comunica la parte izquierda y derecha del corazón por su parte inferior.
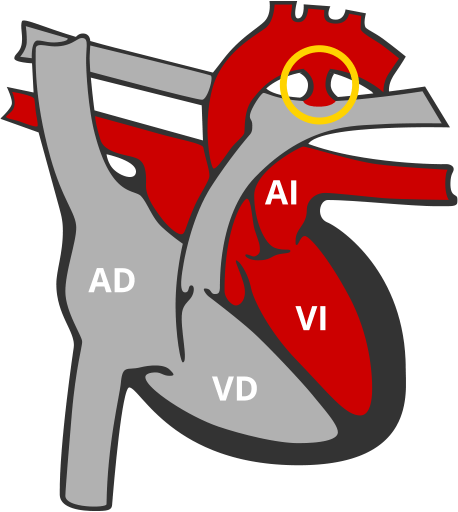
Ductus Arterioso Persistente (DAP)
Comunicación entre la arteria que reparte sangre a todo el cuerpo y la que lleva la sangre a los pulmones.
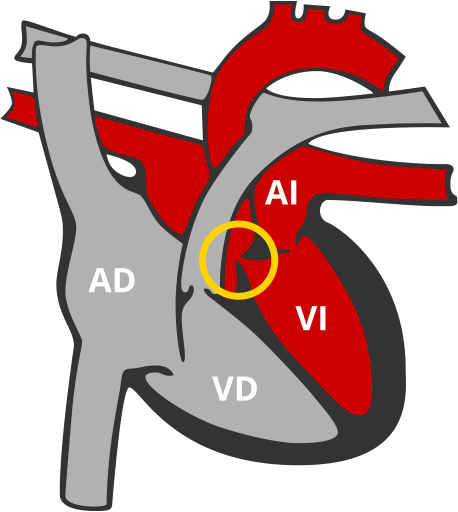
Estenosis Aórtica (EA)
Estrechamiento de la válvula que da paso a la sangre que va del corazón a todo el cuerpo, excepto los pulmones.
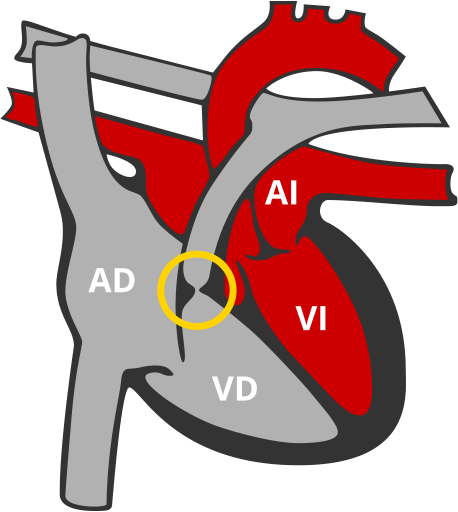
Estenosis Pulmonar (EP)
Estrechamiento de la válvula que da paso a la sangre que va del corazón hacia el pulmón.
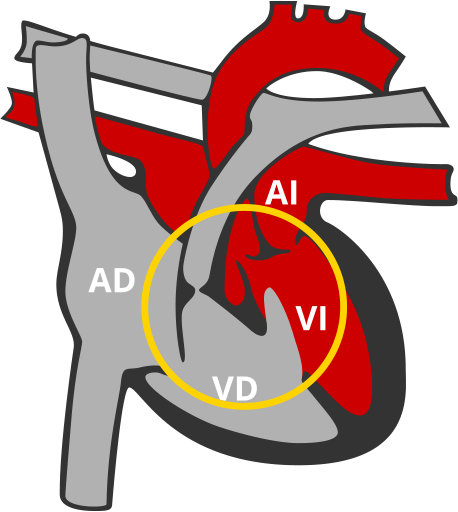
Tetralogía de Fallot
Conjunto de anomalías en el corazón que hacen que la sangre que circula por el cuerpo lleve menos oxígeno de lo normal.
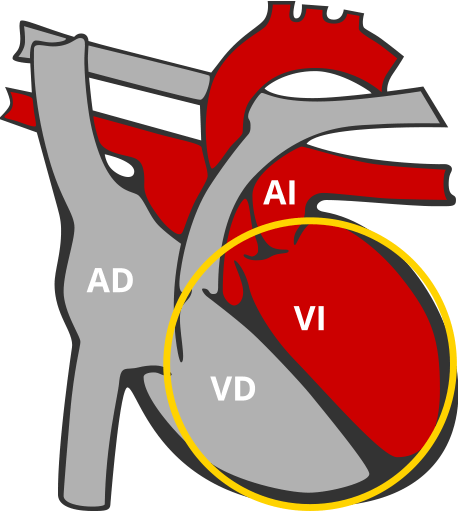
Miocardiopatía dilatada (MCD)
Músculo cardiaco debilitado y ventrículos más grandes de lo habitual.
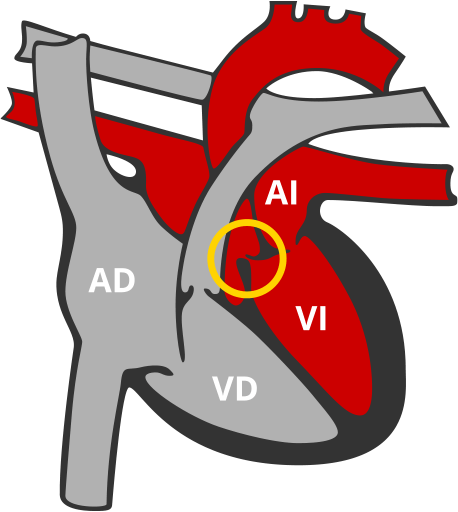
Miocardiopatía hipertrófica (MCH)
Aumento del espesor del músculo cardiaco y reducción de la capacidad de los ventrículos.
Miocardiopatía restrictiva (MCR)
Pérdida de flexibilidad del corazón que disminuye su capacidad de llenado.
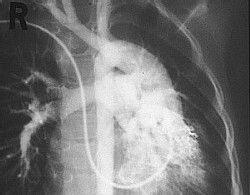
Técnicas de diagnóstico
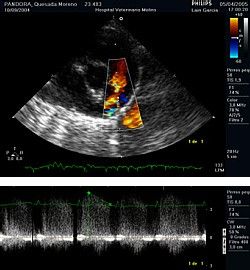
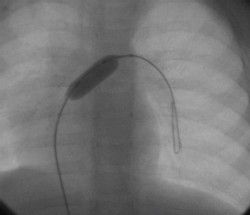
La aparición en los años 80 de la Ecocardiografía 2D con técnica Doppler desplazó el uso del Cateterismo como método más utilizado para el diagnóstico de las enfermedades del corazón.
El cambio de una técnica de alto riesgo, por otra totalmente inocua, supuso una gran revolución para las personas que nacían con cardiopatías congénitas.
Desde entonces, las técnicas de diagnóstico por imagen han evolucionado enormemente y hoy permiten a los expertos estudiar con gran precisión el corazón y sus vasos circundantes.
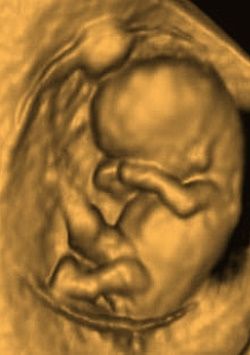
Un ejemplo de innovación en este campo es la Ecocardiografía 3D en tiempo real, que permite obtener imágenes tridimensionales en movimiento.
A la vista de la frecuencia con que se suceden las últimas innovaciones tecnológicas en este campo, podemos asegurar que el futuro de estas técnicas de diagnóstico por imágenes, así como otras de diagnóstico genético, es muy esperanzador.
A continuación, describimos brevemente en qué consiste cada una de las técnicas de diagnóstico. Es muy importante saber a qué procesos va a ser sometido el niño o la niña para evitar angustias innecesarias.
Tratamientos para las cardiopatías congénitas
Una vez diagnosticada la cardiopatía, en muchas ocasiones incluso antes del parto, el cardiólogo pediatra dispone de un amplio abanico de tratamientos para normalizar el funcionamiento del corazón enfermo.
Gracias al desarrollo tecnológico del último siglo, el número de técnicas y recursos es muy amplio, y lo mejor es que no para de crecer. Afortunadamente, podemos afirmar que, hoy día, existen tratamientos para la gran mayoría de cardiopatías congénitas.
En esta sección, explicaremos algunos de estos recursos, entre los que se encuentran los medicamentos, las técnicas quirúrgicas, las prótesis o los marcapasos, entre otros.
Repercusiones de las cardiopatías
Sin pretensión de efectuar una revisión exhaustiva, existe una profusa bibliografía esclarecedora sobre la repercusión de las enfermedades cardíacas en el funcionamiento del sistema nervioso y la frecuente relación de las cardiopatías congénitas con manifestaciones neurológicas adversas1-2-3-4-5-7 de manera que, en general, “las evidencias sugieren que son frecuentes las deficiencias globales del desarrollo, particularmente en la capacidad motora gruesa y fina, lenguaje, razonamiento y trastornos de conducta… siendo también comunes los problemas de aprendizaje y de déficit de atención, así como la necesidad de concurrir a clases especiales o de recibir enseñanza individualizada” 6-7
Como nos señala el trabajo científico realizado por la Asociación Americana del Corazón, “Desde hace varias décadas, se han reducido significativamente las tasas de mortalidad de los niños y adolescentes con CC complejas. Los supervivientes tienen riesgo de morbilidad neurológica causada por factores de riesgo biológicos y medioambientales” 7.
En definitiva, ya sea por algún tipo de complicación neurológica, por haber tenido una lactancia tormentosa con retraso de los hitos del desarrollo psicomotor, hipoxemias originadas por la cardiopatía, hospitalizaciones, las técnicas quirúrgicas complejas a las que son sometidos (con circulación extracorpórea), estancias en UCI y problemas perioperatorios, síndromes esenciales o trastornos genéticos, entorno familiar, ausencias escolares, falta de estimulación temprana, incluso el tipo de apoyo e intervención educativa recibida, la realidad es que los menores y adolescentes afectados por una cardiopatía congénita suelen presentar algunos perfiles característicos, como consecuencia de sufrir una enfermedad permanente y crónica.
No todas las características que presentamos a continuación están presentes en cada menor, sino que hace falta conocer y analizar las secuelas de la cardiopatía congénita en cada caso, independientemente del diagnóstico concreto.
Las repercusiones generales que pueden presentar algunos de los menores afectados por una cardiopatía congénita atendiendo al área de desarrollo son las siguientes:
- Talla inferior.
- Etapas de bajo nivel de oxigenación (anoxias).
- Ritmo de vida lenta.
- En algunos casos, altos niveles de fatiga.
- Etapas con capacidad de respiración disminuida.
- Dificultades visuales.
- Dificultades neurológicas.
- Problemas osteomusculares.
- Síntomas de cianosis: labios y uñas azules
- Retraso madurativo.
- Pocas habilidades motrices.
- Dificultades de escritura y tareas que requieren motricidad fina.
- Dificultades en la orientación temporo-espacial.
- Retraso en la adquisición del lenguaje.
- Dificultades de lecto-escritura.
- Dificultades en la escritura del lenguaje.
- Dificultades de pronunciación: omisión de fonemas, dificultades para emitir determinados fonemas.
- Dificultades de aprendizaje.
- Dificultades de atención y concentración.
- Baja inteligencia (intervenciones extracorpóreas, anoxias…).
- Falta de estimulación temprana.
- Estancias prolongadas en ambientes de estrés psicológicos y emocional.
- Poca tolerancia a la frustración.
- Baja motivación para los aprendizajes.
- Angustias y miedos infantiles (conductas regresivas).
- Alopecia Mutismo selectivo o generalizado.
- Somatizaciones.
- Baja autoestima.
- Sentimientos de vulnerabilidad y de inseguridad, dificultades de regulación emocional.
- Construcciones del autoconcepto en función de ser un niño débil, enfermo y diferente a otros.
- Dificultades para relacionarse con sus iguales (apego ansioso-ambivalente/ansioso-evitativo).
- Agresividad.
- Falta de control de los impulsos.
- “Complejos” con respecto a su físico, especialmente las chicas, a sus capacidades y aptitudes, etc…
- Del sueño.
- De la alimentación.
- Trastornos de déficit de atención con y sin hiperactividad.
- Ansiedad generalizada.
- Falta de aceptación de la propia condición de persona con una enfermedad crónica (no conciencia- de enfermedad/negación).
- Falta de adquisición de hábitos saludables, adaptados a sus limitaciones.
- Conductas de riesgo (consumo de sustancias psicoactivas).
- Falta de autonomía personal.
- Dificultades para la búsqueda de trabajo por falta de preparación académica (el 45% no finalizan los estudios).
- Desestructuración familiar (ansiedad generalizada, irritabilidad, conductas de sobreprotección y, consecuentemente, desatención hacia los demás hijos/as, conductas inductoras en los hijos/as de estigma de enfermedad, estado de ánimo deprimido).
- Embarazos de riesgo.
(1) Complicaciones neurológicas del paciente con cardiopatía (R. Palencia).
(2) Los recién nacidos a término con cardiopatías congénitas tiene anomalías cerebrales extensas (Abnormal Brain Development in Newborns with Congenital Heart Disease. Miller SP, McQuillen PS, Hamrick S, Xu D, Glidden DV, Charlton N, Karl T, Azakie A, Ferriero DM, Barkovich AJ, Vigneron DB).
(3) Impacto de las cardiopatías congénitas en el desarrollo cerebral y el resultado del neurodesarrollo (Donofrio M.T., Massaro AN – Impact of Congenital Heart Disease on Brain Development and Neurodevelopmental Outcome–)
(4) Cardiopatía congénita, cirugía cardíaca y el desarrollo del cerebro
(5) Frequency, Predictors, and Neurologic Outcomes of Vaso-occlusive Strokes Associated With Cardiac Surgery in Children (Trish Domi, David S. Edgell, Brian W. McCrindle, William G. Williams, Anthony K. Chan, Daune L. MacGregor, Adam Kirton, Gabrielle A. deVeber)
(6) Limitaciones funcionales en niños con cardiopatías congénitas después tras una cirugía cardíaca (Functional Limitations in Young Children With Congenital Heart Defects After Cardiac Surgery -Catherine Limperopoulos, Annette Majnemer, Michael I. Shevell, Bernard Rosenblatt, Charles Rohlicek, Christo Tchervenkov, H.Z. Darwish-)
(7) Resultados del desarrollo neurológico en los niños con cardiopatía congénita: Evaluación y manejo (Neurodevelopmental Outcomes in Children With Congenital Heart Disease: Evaluation and Management. A Scientific Statement From the American Heart Association)
(8) Impacto de las cardiopatías congénitas en el sistema nervioso central (Ruiz Romero, Aina)